2020.02.27
人類の「タンパク質枯渇危機」を解決!?ゲノム編集で実現した近大の肉厚マダイ

- Kindai Picks編集部
4457 View
最近、ニュースなどで「ゲノム編集」という言葉を目にすることが増えています。これまでも生き物を人間にとって便利に作り変える技術には、「交配」や「遺伝子組み換え」がありましたが、ゲノム編集はいったいそれらとどう違うのでしょうか? そんな疑問を、近畿大学の水産科学研究所でゲノム編集を使って「肉厚マダイ」を生み出した、家戸敬太郎教授にお聞きしました。
この記事をシェア
近畿大学水産研究所 教授
1967年大阪府東大阪市生まれ。1992年、近畿大学大学院農学研究科修士課程を修了。1993年から近畿大学水産研究所助手、2002年から同講師、2006年から同助教授を経て2014年から同教授。同研究所白浜実験場長および富山実験場長を兼務。
食用の養殖タイは、ぜんぶ近大が起源

――まずはじめに、これまでの生物を作り変える技術と、「ゲノム編集」はどのように違うのか、教えていただけますでしょうか。
人間はこれまで、自然の植物や動物を、自分たちの生活に役立つように改変してきた長い歴史があります。そのために古くから使われてきたのが「交配」という方法です。植物なら大きな実をつける野菜同士の間で受粉させたり、牛の場合なら、よく乳を出す個体の子ども同士を掛け合わせることで、何代もかけて目的に合った性質を持つ品種を作り出してきました。たとえば皆さんが食卓でよく目にする、※キャベツ、ブロッコリー、カリフラワーは、もともと1種類の野草※を品種改良することでできた野菜なんです。
※3種類ともアブラナ科の植物。古代よりヨーロッパで食べられていたキャベツの原種が交雑を経るうちに、突然変異で開花前の花蕾が肥大化するものが生まれ、それを品種改良することで現在のブロッコリー、カリフラワーができた。(諸説あり)
――そうなんですか。見た目も味も大きく違うのに、もとは一つなんですね。
はい。野菜ではトマトも品種改良の産物です。もともとは南米が原産で、原種はとても小さな実しかつけない植物でした。それがメキシコをはじめ世界中で、長い年月をかけて交配を繰り返すことで今のような赤い大きな実をつけるようになったのです。
動物の場合、もっともわかりやすいのはイヌですね。ブルドッグ、チワワ、セントバーナード、柴犬。それぞれ見かけはまったく違いますが、生物種としてはすべて同じです。だから体格のまったく違うセントバーナードとチワワの間でも、理論上は子を成すことができます。
――先生が研究する魚はどうでしょうか。
魚類においても品種改良は古くから行われてきました。観賞魚の代表格である金魚は、紀元前の時代から野生のフナの中から色や形が珍しいものを選んで交配することで今の姿になっていますし、日本では200年以上前から、天然のコイを掛け合わせることで観賞用のニシキゴイを作っています。そんなふうに「育種」※でも、時間をかければ相当に大きさや色を変えることができて、人間に都合の良い生き物を生み出すことができるんですね。
※生物のもつ遺伝的性質を有効活用し、人にとって利用価値のある作物や家畜の新種を、人為的に生成したり改良したりすること
食用魚でいえば、じつは今、皆さんが食べているタイはほぼすべて、私たち近畿大学が生み出した品種がもとになっています。近大では1960年代の前半から早く成長するタイを親にして、何世代もかけて養殖に適したタイを作ってきました。その結果、それまでタイの天然の稚魚が出荷できる大きさの1kgになるまで、3年程かかっていたのが、今では1年半で出荷できるようになっています。全国でマダイの養殖に用いられている稚魚を遡ると、100%近畿大学産のタイに辿り着くといっても過言ではありません。
――みんな近畿大学産のタイが原産だったんですね……。初めて知りました。
ただしこの方法は大きな問題として、ものすごく時間がかかるんです。タイの養殖では、劇的に体質が変わるまでに、平均すると5世代の交配を繰り返す必要があります。養殖用のタイが沢山卵を産みはじめるのは、4歳ぐらいからなので、5世代交配を繰り返すには、20年もの歳月が必要となります。古典的な育種はいろいろな生物種に応用できて効果も高いのですが、とにかく時間がかかるのが大問題でした。
――なるほど。
遺伝子組換えの大きな問題

そこで次に出てきたのが、生物の遺伝子を操作することによって、品種改良のスピードを早めるという方法です。1970年代ぐらいからはじまった技術ですが、生物の受精卵に、働かせたい遺伝子を外から「マイクロインジェクション」という注射器のような装置を使って入れてやる「遺伝子組換え」という方法が一般的ですね。
その他にも、受精卵に放射線を照射したり、化学薬品を使うことで染色体全体にダメージを与えて、突然変異を起こさせるという方法もあります。たとえば皆さんが今食べてるお米なんかは、この突然変異を起こさせる方法で「風が吹いても倒れない、背が低くて実が沢山なる稲」を選抜して栽培したものです。
――おお、身近なお米も、近代科学の産物なんですね。
はい、そっちの方法は食品衛生法の規制の対象になっていないので、ふつうの品種として流通しています。しかし遺伝子組換えで作られた品種は、消費者のイメージが悪いので、ほとんど食品では流通していません。
20年程前にアメリカで、家畜用のエサとして開発された遺伝子組み換えのトウモロコシが、人間の食べる食品として流通して大問題になったんですね。そのトウモロコシには、害虫を殺す成分を生み出す遺伝子が組み込まれており、その成分が人間にアレルギーを起こす可能性があることから、全米のスーパーでタコスなどの回収騒ぎとなりました。それで一気に世界中で、遺伝子組み換え食品に対するイメージが悪くなったんです。
今現在は、大豆などのわずかな農産物で遺伝子組換えが認められていますが、スーパーに並ぶ大豆製品には、ほとんど「遺伝子組み換えではありません」という表記があるはずです。食用魚の場合、認められてるのはアメリカで成長ホルモンをよく出す遺伝子を入れたサケ一種類だけです。
それに魚の遺伝子組換えにも問題がありまして、非常に効率が悪いんですね。受精卵に組み込みたい遺伝子を入れようとしても、その場所や入れる数を、ほとんど制御できないんです。狙った場所に入らないから、何百回、何千回と実験を繰り返して「たまたま偶然入る」のを待つしかありませんでした。その上、今ならゲノム解析の専用装置で一気にぜんぶ調べられますが、以前は遺伝子がどこにどう入ったか確認するのにも、ものすごく時間がかかってたんですね。効率も悪ければ消費者の反対も強いので、結局、遺伝子組換え食品はほとんど流通しなかったんです。
――遺伝子組み換えって、偶然だよりの技術だったんですね。
それで「狙ったところにきちんと遺伝子を入れたり、狙った遺伝子だけを壊したい」というニーズから生まれたのが、「ゲノム編集」という技術です。
狙い通りの遺伝子改変を可能にしたゲノム編集

ゲノム編集は「編集」という言葉通り、文字で書かれた文章を編集するように、生物の体の「設計図」であるゲノムを書き換える技術です。生物の遺伝情報すべてを意味する「ゲノム」は、DNA(デオキシリボ核酸)がその重要な構成要素となります。DNAは4種類の「塩基」が並んだ構造をとっており、その配列によって、生物のさまざまなタンパク質が合成されます。ゲノム編集は、DNAの「文字」にあたる塩基を、任意の場所で改変するために生み出された技術なのです。
ゲノム編集にも世代がありまして、20年ぐらい前に開発された第1世代の手法が「ZFN(ジンク・フィンガー・ヌクレアーゼ)」という技術です。これは、狙った遺伝子と結合するタンパク質(ジンクフィンガー)をデザインして、それに遺伝子を切る酵素をくっつけて、細胞のなかに送り込むというものになります。
2010年頃になると、これを改良した第2世代の「TALEN(ターレン)」という技術も出てきますが、どちらも目的の分子を作るのがかなり大変で、そのために相当の金銭的なコストも必要なことから、一般になかなか普及しませんでした。
――ふむふむ。
その状況を一気に変えて、世界中に「ゲノム編集」ブームを起こしたのが、2012年に発表された「クリスパー・キャス9」という技術です。
――おお! ついに! 名前からしてすごそう。
第3世代のゲノム編集技術であるクリスパー・キャス9は、ZFNやTALENとは違って、タンパク質ではなく「※RNA」を目的の遺伝子にくっつけるための「ガイド役」にしています。
※RNA:リボ核酸。DNAの遺伝情報を読み取り、その設計図通りのタンパク質を合成するためにDNAを「鋳型」として作られる物質。
高校で生物をとっている人はご存知だと思いますが、RNAは遺伝情報であるDNAから「転写」されて作られ、4種類の「塩基」という物質が基本構成要素になります。タンパク質に比べて、RNAを合成するのは非常に簡単で、ふつうの大学生、院生でもできますし、コストもずっと安いので、またたく間に世界中の大学や研究機関に広がったんですね。
細胞に入れられたクリスパー・キャス9は、デザインされたRNAとぴったりくっつくDNAの配列を勝手に探し出し、そこに取り付くとハサミ役の「キャス9」という酵素が狙った場所でDNAを切断します。そうすることで、そこの遺伝子を働かなくさせたり、切断されたDNAの修復過程で遺伝子を入れ込むことが、ものすごく簡単になったんです。
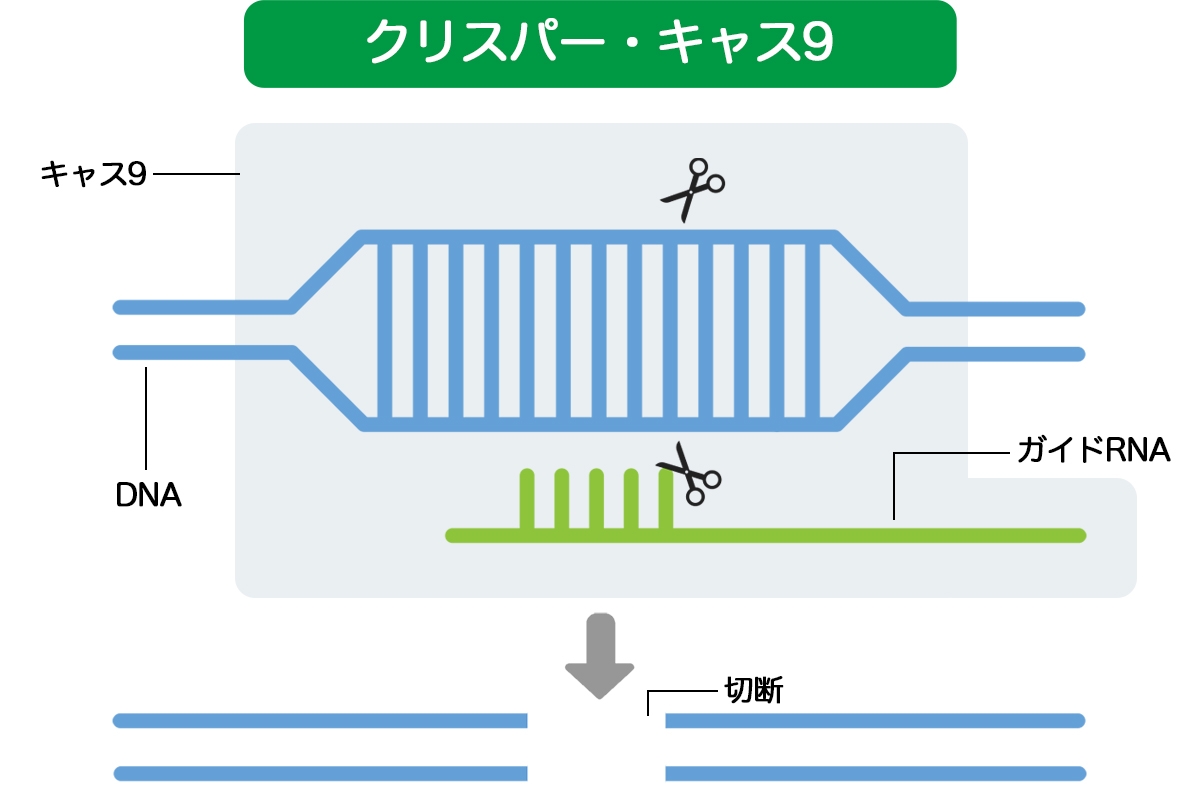
――そういう技術なんですね。新聞で、クリスパー・キャス9の開発者にはノーベル賞が贈られる可能性も高い、と目にしました。
はい、これまで行われていた品種改良や遺伝子組み換えは、時間と手間が膨大にかかる上に偶然任せの技術でした。その改善案として考案されたZFNとTALENは、その合成に高度な技術が必要であり、莫大なコストがかかることから、広く使われるまでに至りませんでした。それに対してクリスパー・キャス9は圧倒的に簡単で効率よく、また正確に遺伝子を編集できる技術だったので、あっという間に広まっていきました。クリスパー・キャス9は医学や生物学の研究をはじめ、創薬や農業、食品生産など幅広い分野に革命をもたらすと期待されています。じつはクリスパー・キャス9のもとになった発見は、日本人の科学者の手によるものなんですよ。
――そうなんですか!
1987年に九州大学の石野良純先生の研究グループが、大腸菌のDNAの中に、正体不明の配列が繰り返し出てくることを論文で発表したのですが、それが「クリスパー」です。じつはその配列は、太古の昔に大腸菌の祖先が、ウィルスなどに感染したときに取り込んだ、ウィルスの遺伝子の一部だったんです。生物には「獲得免疫」と呼ばれる、自分以外の菌やウィルスが体内に入り込んできたときに自動的に認識して殺す仕組みが備わっています。その「敵を認識して殺すためのシステム」の正体が、クリスパーだったと今ではわかっています。
ゲノム編集によって生み出された近大の「肉厚マダイ」

――ここまでの説明で、ゲノム編集がどういう技術なのか、概要が理解できました。それではいよいよ、家戸先生がゲノム編集を使って、どんな研究を進めているのか教えていただけますか?
はい、では我々がゲノム編集を使って生み出した「肉厚マダイ」を見に行きましょう。

先生の後をついて、水産研究所内の実験棟に足を運ぶと、そこには沢山の水槽の中を元気に泳ぐ魚がいました。
――めちゃめちゃ元気ですね! この魚たちはみんなタイですか?
はい、木下先生とともに最初にマダイのゲノム編集に取り組んだのは2014年のことですが、そこから第3世代にあたります。成長スピードも早く、ふつうのマダイに比べると、肉の厚みが1.5倍ぐらいになってるのがわかりますか?
――たしかに分厚くてめちゃマッチョな感じがします……。どういう遺伝子を操作して、こうなったのでしょうか?
タイの受精卵の、ミオスタチンという遺伝子をクリスパー・キャス9で壊すことで、これだけ肉厚に成長しました。ミオスタチンは人間のゲノムにもある、「筋肉がつきすぎないように、その成長を抑制する遺伝子」です。
ベルギーの原産で「ベルジャン・ブルー」という、通常の牛の2倍ぐらいの筋肉をつけるムキムキの食用牛がいるのですが、その牛は突然変異でミオスタチンが壊れていることがわかっていました。ミオスタチンはメダカなどの魚類にも存在していることから、それを壊せば肉厚の魚に成長するだろうと考えたんですね。ゲノム編集したタイを、第2世代、第3世代と養殖するうちに、どんどん通常のタイよりも筋肉量が増えています。
左が普通のマダイで、右が肉厚マダイ。
――これはすごい。ちなみに、先生たちはこのタイを食べたことはあるのでしょうか?
はい、実験に使ったタイは、刺し身や焼き物にして食べてます。まだ実験段階で、食用にするためには、食品会社などとの共同研究が必要ですが、いまはその準備のために成分などの分析をしているところです。味もふつうのタイとほとんど変わりません。筋肉が増えると、それにともなって筋繊維を束ねるコラーゲンの量が相対的に減少すると考えられるので若干もっちりとした歯ごたえが強まる感じはありますが、美味しく食べられます。
含まれる栄養価や成分の分析とともに、万が一のことがあってはいけませんので、有害な毒素やアレルゲンなどが含まれていないか調べているところですが、今のところ食用として流通しても問題ないだろうと考えています。

――でも、これだけ大きくなるということは、その分、ふつうのタイより沢山エサが必要になるんですよね。そうなると、養殖のコストが上がってしまうのでは……。
ところが、エサを食べる量もふつうのマダイとあまり変わらないんです。取り込んだ栄養素を筋肉へと変換する効率が、ミオスタチンの破壊によって上がっていると考えられますね。タイという魚は、硬い骨が多いので、一匹のうち食べられるのは身の40%しかないんですね。養殖ブリの場合は可食部が身の60%と多いので、タイに比べて養殖の効率がいいんです。この技術によって、タイもブリ並に養殖効率が上げられるだろうと考えています。
――すごいですね。タイ以外の食用魚類、食用動物にもこの技術を応用することはできるのでしょうか?
はい、おそらく可能ですし、世界中の研究者があちこちでそれに挑んでいます。今世界では、増え続ける人口に対して、将来的に「タンパク質が足りなくなるのではないか」と懸念されています。人間が健康的に生きていくためには、米や小麦などの穀類、ビタミンを含む野菜の他に、良質なタンパク質をとることが必須となります。ところが食用肉のための家畜の成長、魚の養殖のためには、大量のエサが必要になるので、農業生産よりもはるかに多くのコストがかかるんですね。
アジアやアフリカの国々もどんどん経済成長を続けていますが、国が豊かになるとともに、動物性タンパク質の消費量が上がっていくことは確実です。「未来のタンパク質食糧危機」を解決するための一つの手段として、ゲノム編集による食用動物の生産効率化は、非常に有効な方法だと考えています。
――ゲノム編集が、世界の食糧危機を救うかもしれない、大きな可能性を秘めた技術であることが家戸先生の話でよく理解できました。これからのさらなるご研究の成果を、楽しみにしております!
(終わり)
取材・文:大越裕(チーム・パスカル)
写真:黒川直樹
編集・企画:人間編集部
この記事をシェア











